您现在的位置是: 首页 > 招生信息 招生信息
天津2014年高考化学_2014年天津化学高考题
tamoadmin 2024-05-27 人已围观
简介1.天津化学赋分90多难2.2023天津高考考几天3.今年天津高考时间20234.天津高考人数2023年多少人5.求对高考化学无机推断题有帮助的(天津地区常考的)历史容易得赋分。在未进行新高考选科之前,学霸,普通生和差生都会学习化学。在自由选科之后,成绩不好的学生都不会再选择化学,因此选择化学的学生都是学霸,竞争会十分激烈,如果成绩不好的话选化学很容易沦为垫底,最后赋分很低,而历史赋分能赋分到10
1.天津化学赋分90多难
2.2023天津高考考几天
3.今年天津高考时间2023
4.天津高考人数2023年多少人
5.求对高考化学无机推断题有帮助的(天津地区常考的)

历史容易得赋分。在未进行新高考选科之前,学霸,普通生和差生都会学习化学。在自由选科之后,成绩不好的学生都不会再选择化学,因此选择化学的学生都是学霸,竞争会十分激烈,如果成绩不好的话选化学很容易沦为垫底,最后赋分很低,而历史赋分能赋分到100分的,裸分得八九十分,不会低于80。
天津化学赋分90多难
2023年天津高考时间时间表如下:
6月7日:09:00-11:30语文,15:00-17:00数学;6月8日:15:00-16:40英语笔试,15:00-17:00外语;
6月9日:08:30-09:30物理,11:00-12:00思想政治,15:00-16:00化学。
6月10日:08:30-09:30历史,11:00-12:00生物学,15:00-16:00地理。
资料扩展:
天津省海岸线位于渤海西部海域,南起歧口,北至涧河口,长达153千米。有滩涂资源、海洋生物资源、海水资源、海洋油气资源。滩涂面积约370多平方千米,已开发利用。海洋生物资源,主要是浮游生物、游泳生物、底栖生物和潮间带生物。
海水成盐量高,自古以来就是著名的盐产地,拥有中国最大的盐场。进行海水淡化,解决淡水不足的潜力很大。截至2016年,已发现45个含油构造,储量十分可观。天津有约153千米的海岸线,拥有中国最著名的海盐产区长芦盐场。
天津地区植被大致可分为针叶林、针阔叶混交林、落叶阔叶林、灌草丛、草甸、盐生植被、沼泽植被、水生植被、沙生植被、人工林、农田种植植物等11种。
渔业资源种类约有80多种,主要渔获种类有30多种。加强野生动物及其栖息地保护,截至2020年,我市共观测记录鸟类452种,较2014年记录种类增加了36种。
天津是一个多民族散居、杂居的沿海城市。根据第七次全国人口普查统计,常住人口中,汉族人口为13422528人,占96.80%;各少数民族人口为443481人,占3.20%。同2010年第六次全国人口普查相比,汉族人口增加815252人,增长6.47%。
2023天津高考考几天
需要在天津市排名在10%之内。赋分和排名有关,但卷子难体现排名的优势。大家都是50-60分,60分有可能赋分到90多分,而50分则有可能赋分到七八十分。查原始分没有意义,只能知道自己的排名大概是什么位次。要想赋分到90分以上,需要在天津市排名在10%之内,且是三分一赋制。
今年天津高考时间2023
2023年天津高考为6月7日至9日,共计3天。下面将对天津高考的时间、科目以及注意事项进行详细介绍。
一、考试时间
天津高考时间为6月7日至9日,其中6月7日为语文科目考试,6月8日为数学科目考试,6月9日为英语科目考试。考试时间均为上午9:00-11:30和下午3:00-5:30两个时间段。
二、考试科目
天津高考科目包括语文、数学和英语三门必考科目,此外还有选考科目。2023年天津高考的选考科目包括物理、化学、生物、历史、地理、政治、技术及艺术等8个科目,考生可根据自身兴趣和特长进行选择。
三、考场安排
考生需要在规定时间内到达考场,并携带好相关证件和材料,如准考证、身份证、文具等。考生需在考试前20分钟进入考场,到考场后需要听从监考老师的指示,服从考场管理和监督。
四、考试注意事项
考生在考试过程中需要注意以下几点:1.严格遵守考场纪律;2.认真审核准考证和材料;3.按照考场规定使用文具和答题卡;4.注意填涂答案的正确方式和步骤;5.不要在答题卡、试卷、草稿纸上乱涂乱写。
五、高考复读与志愿填报
对于没有达到心仪大学录取分数线的考生,可以选择复读。高考复读需要制定具体的复读计划,注重基础知识的夯实以及技巧的掌握,同时也要注意身体和心理的调节。复读后,考生需要重新参加高考,并填报志愿。志愿填报需要了解各大学的专业设置和录取要求,结合自身兴趣和特长进行选择。
六、高考成绩与录取
高考成绩是考生申请大学的重要参考依据之一。高考成绩通常在7月份公布,考生需要及时查看成绩并核对。同时,考生还需要关注各大学的录取情况,了解自己的录取情况并及时提交材料。
总之,高考是人生中非常重要的一场考试,需要考生们严肃对待。只有科学备考、认真考试、合理填报志愿才能更好地实现自己的人生价值。
天津高考人数2023年多少人
今年天津高考时间2023如下:
天津市2023年高考时间已经确定,将于6月7日至9日进行,考试科目为语文、数学、英语和综合科目。下面详细介绍天津市2023年高考时间表,供大家参考。
一、报名时间
报名时间通常在高考前4个月进行。根据以往惯例,2023年的天津市高考报名时间可能在2月份左右,确切的时间将在教育部门的相关公告中发布。
二、填报志愿时间
考生在完成高考报名后,需要在规定时间内进行填报志愿。由于2023年高考时间为6月7日至9日,所以按照以往的规律,填报志愿的时间应该是在高考结束之后,也就是6月10日至13日。
三、高考时间
1、6月7日(周三)上午8:00-11:00语文
2、6月7日(周三)下午14:30-17:30数学(文)政治(理)
3、6月8日(周四)上午8:00-11:00英语
4、6月8日(周四)下午14:30-17:30化学(文)历史(理)
5、6月9日(周五)上午8:00-11:00物理(文)地理(理)
6、6月9日(周五)下午14:30-17:30综合科目
四、成绩查询时间
考生完成高考后,需要等待相关部门公布成绩。根据惯例,2023年天津市高考成绩查询时间将在7月份左右,具体时间则需要等到教育部门的相关公告。
五、志愿填报时间
在获取考试成绩之后,考生需要在规定时间内进行志愿填报。经过数次调查,前两个工作日为大概率,填报时间应该是在7月11日至7月12日左右。
六、录取时间
填报志愿之后,考生需要等待高校录取结果。录取时间通常在8月份左右,也就是说,考生可以在8月底或者9月初收到录取通知书。
以上是天津市2023年高考的时间表。虽然具体时间还未确定,但这些时间都是在以往时间的基础上推测出来的,可以作为考生和家长参考的依据。同时,在考试过程中,考生需要保持良好的心态,严格遵守考场纪律和规定,才能发挥自己的最佳水平,取得好的成绩。
求对高考化学无机推断题有帮助的(天津地区常考的)
天津高考人数2023年多少人介绍如下:
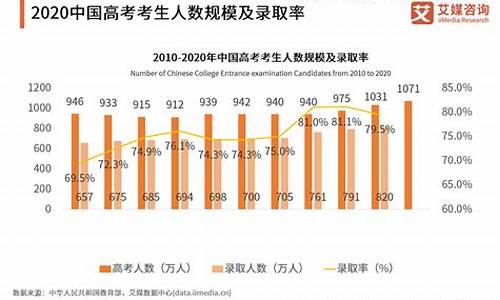
2023天津高考报名人数是6.9万人,天津高考使用的是自主命题卷。天津2023年普通高考将于6月7日、8日举行,普通高中学业水平等级性考试将于6月9日、10日举行。
历年天津高考报名人数:
1、2022年天津高考人数:天津市2022年的报名人数约为5.8万,比去年增加了约2千人,增幅约为3.6%。
2、2021年天津高考人数:2021 年天津市高考报名人数是5.6万余人。
3、2020年天津高考人数:2020年天津 市普通高考共报名5.6万余人。
天津高考各科分值:
1、天津高考语文、数学、外语3门为统一高考科目,每门150分,其中外语听力考试满分30分,取两次听力考试的最高成绩与其他部分试题成绩一同组成外语科目成绩计入高考总分。
2、普通高中学业水平等级性考试科目又叫“学考等级考”科目有:思想政治、历史、地理、物理、化学、生物六门,由天津考生自主选择3|参加考试,每科目满分100分,三门即300分。
天津高考注意事项:
1、高考时间的合理运用:天津考生要合理利用每道题目规定的作答时间,对每个试题作答要围绕要点,避免花费过多时间,以完成所有的试题。
2、高考交卷前再检查:天津考生在交卷前要再次检查每道题目,看是否有遗漏或需要修改的地方。也检查答题卡信息是否填涂准确,以确保成绩的准确性。
3、高考结束不得在考场逗留:天津考生考试结束要立即离开考场,不得在考场或考点停留,以免引起不必要的麻烦。
自主命题试卷的含义
1、2023天津高考使用自主命题试卷,高考自主命题即是各个省份可以不使用教育部编写的全国试卷,单独组织本省教师进行考试试卷的编写,即自主进行高考试卷的单独命题。
2、高考后试卷不能拿走,高考试卷会密封后送到指定的阅卷场所,阅卷后的高考试卷属于高考档案的一种,要存档保留一定年限的,考生是无法再次接触到自己的高考试卷的。
3、自主命题卷适用于北京市、上海市、 天津市等。
常见方程式
非金属单质(F2 ,Cl2 , O2 , S, N2 , P , C , Si)
1, 氧化性:
F2 + H2 === 2HF
F2 +Xe(过量)===XeF2
2F2(过量)+Xe===XeF4
nF2 +2M===2MFn (表示大部分金属)
2F2 +2H2O===4HF+O2
2F2 +2NaOH===2NaF+OF2 +H2O
F2 +2NaCl===2NaF+Cl2
F2 +2NaBr===2NaF+Br2
F2+2NaI ===2NaF+I2
F2 +Cl2 (等体积)===2ClF
3F2 (过量)+Cl2===2ClF3
7F2(过量)+I2 ===2IF7
Cl2 +H2 ===2HCl
3Cl2 +2P===2PCl3
Cl2 +PCl3 ===PCl5
Cl2 +2Na===2NaCl
3Cl2 +2Fe===2FeCl3
Cl2 +2FeCl2 ===2FeCl3
Cl2+Cu===CuCl2
2Cl2+2NaBr===2NaCl+Br2
Cl2 +2NaI ===2NaCl+I2
5Cl2+I2+6H2O===2HIO3+10HCl
Cl2 +Na2S===2NaCl+S
Cl2 +H2S===2HCl+S
Cl2+SO2 +2H2O===H2SO4 +2HCl
Cl2 +H2O2 ===2HCl+O2
2O2 +3Fe===Fe3O4
O2+K===KO2
S+H2===H2S
2S+C===CS2
S+Fe===FeS
S+2Cu===Cu2S
3S+2Al===Al2S3
S+Zn===ZnS
N2+3H2===2NH3
N2+3Mg===Mg3N2
N2+3Ca===Ca3N2
N2+3Ba===Ba3N2
N2+6Na===2Na3N
N2+6K===2K3N
N2+6Rb===2Rb3N
P2+6H2===4PH3
P+3Na===Na3P
2P+3Zn===Zn3P2
2.还原性
S+O2===SO2
S+O2===SO2
S+6HNO3(浓)===H2SO4+6NO2+2H2O
3S+4 HNO3(稀)===3SO2+4NO+2H2O
N2+O2===2NO
4P+5O2===P4O10(常写成P2O5)
2P+3X2===2PX3 (X表示F2,Cl2,Br2)
PX3+X2===PX5
P4+20HNO3(浓)===4H3PO4+20NO2+4H2O
C+2F2===CF4
C+2Cl2===CCl4
2C+O2(少量)===2CO
C+O2(足量)===CO2
C+CO2===2CO
C+H2O===CO+H2(生成水煤气)
2C+SiO2===Si+2CO(制得粗硅)
Si(粗)+2Cl===SiCl4
(SiCl4+2H2===Si(纯)+4HCl)
Si(粉)+O2===SiO2
Si+C===SiC(金刚砂)
Si+2NaOH+H2O===Na2SiO3+2H2
,(碱中)歧化
Cl2+H2O===HCl+HClO
(加酸抑制歧化,加碱或光照促进歧化)
Cl2+2NaOH===NaCl+NaClO+H2O
2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
3Cl2+6KOH(热,浓)===5KCl+KClO3+3H2O
3S+6NaOH===2Na2S+Na2SO3+3H2O
4P+3KOH(浓)+3H2O===PH3+3KH2PO2
11P+15CuSO4+24H2O===5Cu3P+6H3PO4+15H2SO4
3C+CaO===CaC2+CO
3C+SiO2===SiC+2CO
二,金属单质(Na,Mg,Al,Fe)的还原性
2Na+H2===2NaH
4Na+O2===2Na2O
2Na2O+O2===2Na2O2
2Na+O2===Na2O2
2Na+S===Na2S(爆炸)
2Na+2H2O===2NaOH+H2
2Na+2NH3===2NaNH2+H2
4Na+TiCl4(熔融)===4NaCl+Ti
Mg+Cl2===MgCl2
Mg+Br2===MgBr2
2Mg+O2===2MgO
Mg+S===MgS
Mg+2H2O===Mg(OH)2+H2
2Mg+TiCl4(熔融)===Ti+2MgCl2
Mg+2RbCl===MgCl2+2Rb
2Mg+CO2===2MgO+C
2Mg+SiO2===2MgO+Si
Mg+H2S===MgS+H2
Mg+H2SO4===MgSO4+H2
2Al+3Cl2===2AlCl3
4Al+3O2===2Al2O3(钝化)
4Al(Hg)+3O2+2xH2O===2(Al2O3.xH2O)+4Hg
4Al+3MnO2===2Al2O3+3Mn
2Al+Cr2O3===Al2O3+2Cr
2Al+Fe2O3===Al2O3+2Fe
2Al+3FeO===Al2O3+3Fe
2Al+6HCl===2AlCl3+3H2
2Al+3H2SO4===Al2(SO4)3+3H2
2Al+6H2SO4(浓)===Al2(SO4)3+3SO2+6H2O
(Al,Fe在冷,浓的H2SO4,HNO3中钝化)
Al+4HNO(稀)===Al(NO3)3+NO+2H2O
2Al+2NaOH+2H2O===2NaAlO2+3H2
2Fe+3Br2===2FeBr3
Fe+I2===FeI2
Fe+S===FeS
3Fe+4H2O(g)===Fe3O4+4H2
Fe+2HCl===FeCl2+H2
Fe+CuCl2===FeCl2+Cu
Fe+SnCl4===FeCl2+SnCl2
(铁在酸性环境下,不能把四氯化锡完全
还原为单质锡 Fe+SnCl2==FeCl2+Sn)
三, 非金属氢化物(HF,HCl,H2O,H2S,NH3)
1,还原性:
4HCl(浓)+MnO2===MnCl2+Cl2+2H2O
4HCl(g)+O2===2Cl2+2H2O
16HCl+2KMnO4===2KCl+2MnCl2+5Cl2+8H2O
14HCl+K2Cr2O7===2KCl+2CrCl3+3Cl2+7H2O
2H2O+2F2===4HF+O2
2H2S+3O2(足量)===2SO2+2H2O
2H2S+O2(少量)===2S+2H2O
2H2S+SO2===3S+2H2O
H2S+H2SO4(浓)===S+SO2+2H2O
3H2S+2HNO(稀)===3S+2NO+4H2O
5H2S+2KMnO4+3H2SO4===2MnSO4+K2SO4+5S+8H2O
3H2S+K2Cr2O7+4H2SO4===Cr2(SO4)3+K2SO4+3S+7H2O
H2S+4Na2O2+2H2O===Na2SO4+6NaOH
2NH3+3CuO===3Cu+N2+3H2O
2NH3+3Cl2===N2+6HCl
8NH3+3Cl2===N2+6NH4Cl
4NH3+3O2(纯氧)===2N2+6H2O
4NH3+5O2===4NO+6H2O
4NH3+6NO===5N2+6HO(用氨清除NO)
NaH+H2O===NaOH+H2
4NaH+TiCl4===Ti+4NaCl+2H2
CaH2+2H2O===Ca(OH)2+2H2
2,酸性:
4HF+SiO2===SiF4+2H2O
(此反应广泛应用于测定矿样或钢样中SiO2的含量)
2HF+CaCl2===CaF2+2HCl
H2S+Fe===FeS+H2
H2S+CuCl2===CuS+2HCl
H2S+2AgNO3===Ag2S+2HNO3
H2S+HgCl2===HgS+2HCl
H2S+Pb(NO3)2===PbS+2HNO3
H2S+FeCl2===
2NH3+2Na==2NaNH2+H2
(NaNH2+H2O===NaOH+NH3)
3,碱性:
NH3+HCl===NH4Cl
NH3+HNO3===NH4NO3
2NH3+H2SO4===(NH4)2SO4
NH3+NaCl+H2O+CO2===NaHCO3+NH4Cl
(此反应用于工业制备小苏打,苏打)
4,不稳定性:
2HF===H2+F2
2HCl===H2+Cl2
2H2O===2H2+O2
2H2O2===2H2O+O2
H2S===H2+S
2NH3===N2+3H2
四,非金属氧化物
低价态的还原性:
2SO2+O2===2SO3
2SO2+O2+2H2O===2H2SO4
(这是SO2在大气中缓慢发生的环境化学反应)
SO2+Cl2+2H2O===H2SO4+2HCl
SO2+Br2+2H2O===H2SO4+2HBr
SO2+I2+2H2O===H2SO4+2HI
SO2+NO2===SO3+NO
2NO+O2===2NO2
NO+NO2+2NaOH===2NaNO2
(用于制硝酸工业中吸收尾气中的NO和NO2)
2CO+O2===2CO2
CO+CuO===Cu+CO2
3CO+Fe2O3===2Fe+3CO2
CO+H2O===CO2+H2
氧化性:
SO2+2H2S===3S+2H2O
SO3+2KI===K2SO3+I2
NO2+2KI+H2O===NO+I2+2KOH
(不能用淀粉KI溶液鉴别溴蒸气和NO2)
4NO2+H2S===4NO+SO3+H2O
2NO2+Cu===4CuO+N2
CO2+2Mg===2MgO+C
(CO2不能用于扑灭由Mg,Ca,Ba,Na,K等燃烧的火灾)
SiO2+2H2===Si+2H2O
SiO2+2Mg===2MgO+Si
3,与水的作用:
SO2+H2O===H2SO3
SO3+H2O===H2SO4
3NO2+H2O===2HNO3+NO
N2O5+H2O===2HNO3
P2O5+H2O===2HPO3
P2O5+3H2O===2H3PO4
(P2O5极易吸水,可作气体干燥剂
P2O5+3H2SO4(浓)===2H3PO4+3SO3)
CO2+H2O===H2CO3
4,与碱性物质的作用:
SO2+2NH3+H2O===(NH4)2SO3
SO2+(NH4)2SO3+H2O===2NH4HSO3
(这是硫酸厂回收SO2的反应.先用氨水吸收SO2,
再用H2SO4处理: 2NH4HSO3+H2SO4===(NH4)2SO4+2H2O+2SO2
生成的硫酸铵作化肥,SO2循环作原料气)
SO2+Ca(OH)2===CaSO3+H2O
(不能用澄清石灰水鉴别SO2和CO2.可用品红鉴别)
SO3+MgO===MgSO4
SO3+Ca(OH)2===CaSO4+H2O
CO2+2NaOH(过量)===Na2CO3+H2O
CO2(过量)+NaOH===NaHCO3
CO2+Ca(OH)2(过量)===CaCO3+H2O
2CO2(过量)+Ca(OH)2===Ca(HCO3)2
CO2+2NaAlO2+3H2O===2Al(OH)3+Na2CO3
CO2+C6H5ONa+H2O===C6H5OH+NaHCO3
SiO2+CaO===CaSiO3
SiO2+2NaOH===Na2SiO3+H2O
(常温下强碱缓慢腐蚀玻璃)
SiO2+Na2CO3===Na2SiO3+CO2
SiO2+CaCO3===CaSiO3+CO2
五,金属氧化物
1,低价态的还原性:
6FeO+O2===2Fe3O4
FeO+4HNO3===Fe(NO3)3+NO2+2H2O
2,氧化性:
Na2O2+2Na===2Na2O
(此反应用于制备Na2O)
MgO,Al2O3几乎没有氧化性,很难被还原为Mg,Al.
一般通过电解制Mg和Al.
Fe2O3+3H2===2Fe+3H2O (制还原铁粉)
Fe3O4+4H2===3Fe+4H2O
3,与水的作用:
Na2O+H2O===2NaOH
2Na2O2+2H2O===4NaOH+O2
(此反应分两步:Na2O2+2H2O===2NaOH+H2O2 ;
2H2O2===2H2O+O2. H2O2的制备可利用类似的反应:
BaO2+H2SO4(稀)===BaSO4+H2O2)
MgO+H2O===Mg(OH)2 (缓慢反应)
4,与酸性物质的作用:
Na2O+SO3===Na2SO4
Na2O+CO2===Na2CO3
Na2O+2HCl===2NaCl+H2O
2Na2O2+2CO2===2Na2CO3+O2
Na2O2+H2SO4(冷,稀)===Na2SO4+H2O2
MgO+SO3===MgSO4
MgO+H2SO4===MgSO4+H2O
Al2O3+3H2SO4===Al2(SO4)3+3H2O
(Al2O3是两性氧化物:
Al2O3+2NaOH===2NaAlO2+H2O)
FeO+2HCl===FeCl2+3H2O
Fe2O3+6HCl===2FeCl3+3H2O
Fe2O3+3H2S(g)===Fe2S3+3H2O
Fe3O4+8HCl===FeCl2+2FeCl3+4H2O
六,含氧酸
1,氧化性:
4HClO3+3H2S===3H2SO4+4HCl
HClO3+HI===HIO3+HCl
3HClO+HI===HIO3+3HCl
HClO+H2SO3===H2SO4+HCl
HClO+H2O2===HCl+H2O+O2
(氧化性:HClO>HClO2>HClO3>HClO4,
但浓,热的HClO4氧化性很强)
2H2SO4(浓)+C===CO2+2SO2+2H2O
2H2SO4(浓)+S===3SO2+2H2O
H2SO4+Fe(Al) 室温下钝化
6H2SO4(浓)+2Fe===Fe2(SO4)3+3SO2+6H2O
2H2SO4(浓)+Cu===CuSO4+SO2+2H2O
H2SO4(浓)+2HBr===SO2+Br2+2H2O
H2SO4(浓)+2HI===SO2+I2+2H2O
H2SO4(稀)+Fe===FeSO4+H2
2H2SO3+2H2S===3S+2H2O
4HNO3(浓)+C===CO2+4NO2+2H2O
6HNO3(浓)+S===H2SO4+6NO2+2H2O
5HNO3(浓)+P===H3PO4+5NO2+H2O
6HNO3+Fe===Fe(NO3)3+3NO2+3H2O
4HNO3+Fe===Fe(NO3)3+NO+2H2O
30HNO3+8Fe===8Fe(NO3)3+3N2O+15H2O
36HNO3+10Fe===10Fe(NO3)3+3N2+18H2O
30HNO3+8Fe===8Fe(NO3)3+3NH4NO3+9H2O
2,还原性:
H2SO3+X2+H2O===H2SO4+2HX
(X表示Cl2,Br2,I2)
2H2SO3+O2===2H2SO4
H2SO3+H2O2===H2SO4+H2O
5H2SO3+2KMnO4===2MnSO4+K2SO4+2H2SO4+3H2O
H2SO3+2FeCl3+H2O===H2SO4+2FeCl2+2HCl
3,酸性:
H2SO4(浓) +CaF2===CaSO4+2HF
H2SO4(浓)+NaCl===NaHSO4+HCl
H2SO4(浓) +2NaCl===Na2SO4+2HCl
H2SO4(浓)+NaNO3===NaHSO4+HNO3
3H2SO4(浓)+Ca3(PO4)2===3CaSO4+2H3PO4
2H2SO4(浓)+Ca3(PO4)2===2CaSO4+Ca(H2PO4)2
3HNO3+Ag3PO4===H3PO4+3AgNO3
2HNO3+CaCO3===Ca(NO3)2+H2O+CO2
(用HNO3和浓H2SO4不能制备H2S,HI,HBr,(SO2)
等还原性气体)
4H3PO4+Ca3(PO4)2===3Ca(H2PO4)2(重钙)
H3PO4(浓)+NaBr===NaH2PO4+HBr
H3PO4(浓)+NaI===NaH2PO4+HI
4,不稳定性:
2HClO===2HCl+O2
4HNO3===4NO2+O2+2H2O
H2SO3===H2O+SO2
H2CO3===H2O+CO2
H4SiO4===H2SiO3+H2O
七,碱
低价态的还原性:
4Fe(OH)2+O2+2H2O===4Fe(OH)3
与酸性物质的作用:
2NaOH+SO2(少量)===Na2SO3+H2O
NaOH+SO2(足量)===NaHSO3
2NaOH+SiO2===NaSiO3+H2O
2NaOH+Al2O3===2NaAlO2+H2O
2NaOH+Cl2===NaCl+NaClO+H2O
NaOH+HCl===NaCl+H2O
NaOH+H2S(足量)===NaHS+H2O
2NaOH+H2S(少量)===Na2S+2H2O
3NaOH+AlCl3===Al(OH)3+3NaCl
NaOH+Al(OH)3===NaAlO2+2H2O
(AlCl3和Al(OH)3哪个酸性强?)
NaOH+NH4Cl===NaCl+NH3+H2O
Mg(OH)2+2NH4Cl===MgCl2+2NH3.H2O
Al(OH)3+NH4Cl 不溶解
3,不稳定性:
Mg(OH)2===MgO+H2O
2Al(OH)3===Al2O3+3H2O
2Fe(OH)3===Fe2O3+3H2O
Cu(OH)2===CuO+H2O
八,盐
1,氧化性:
2FeCl3+Fe===3FeCl2
2FeCl3+Cu===2FeCl2+CuCl2
(用于雕刻铜线路版)
2FeCl3+Zn===2FeCl2+ZnCl2
FeCl3+Ag===FeCl2+AgC
Fe2(SO4)3+2Ag===FeSO4+Ag2SO4(较难反应)
Fe(NO3)3+Ag 不反应
2FeCl3+H2S===2FeCl2+2HCl+S
2FeCl3+2KI===2FeCl2+2KCl+I2
FeCl2+Mg===Fe+MgCl2
2,还原性:
2FeCl2+Cl2===2FeCl3
3Na2S+8HNO3(稀)===6NaNO3+2NO+3S+4H2O
3Na2SO3+2HNO3(稀)===3Na2SO4+2NO+H2O
2Na2SO3+O2===2Na2SO4
3,与碱性物质的作用:
MgCl2+2NH3.H2O===Mg(OH)2+NH4Cl
AlCl3+3NH3.H2O===Al(OH)3+3NH4Cl
FeCl3+3NH3.H2O===Fe(OH)3+3NH4Cl
4,与酸性物质的作用:
Na3PO4+HCl===Na2HPO4+NaCl
Na2HPO4+HCl===NaH2PO4+NaCl
NaH2PO4+HCl===H3PO4+NaCl
Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2
3Na2CO3+2AlCl3+3H2O===2Al(OH)3+3CO2+6NaCl
3Na2CO3+2FeCl3+3H2O===2Fe(OH)3+3CO2+6NaCl
3NaHCO3+AlCl3===Al(OH)3+3CO2
3NaHCO3+FeCl3===Fe(OH)3+3CO2
3Na2S+Al2(SO4)3+6H2O===2Al(OH)3+3H2S
3NaAlO2+AlCl3+6H2O===4Al(OH)3
5,不稳定性:
Na2S2O3+H2SO4===Na2SO4+S+SO2+H2O
NH4Cl===NH3+HCl
NH4HCO3===NH3+H2O+CO2
2KNO3===2KNO2+O2
2Cu(NO3)3===2CuO+4NO2+O2
2KMnO4===K2MnO4+MnO2+O2
2KClO3===2KCl+3O2
2NaHCO3===Na2CO3+H2O+CO2
Ca(HCO3)2===CaCO3+H2O+CO2
CaCO3===CaO+CO2
MgCO3===MgO+CO2
几种重要阳离子的检验
(l)H+ 能使紫色石蕊试液或橙色的甲基橙试液变为红色。
(2)Na+、K+ 用焰色反应来检验时,它们的火焰分别呈**、浅紫色(通过钴玻片)。
(3)Ba2+ 能使稀硫酸或可溶性硫酸盐溶液产生白色BaSO4沉淀,且沉淀不溶于稀硝酸。
(4)Mg2+ 能与NaOH溶液反应生成白色Mg(OH)2沉淀,该沉淀能溶于NH4Cl溶液。
(5)Al3+ 能与适量的NaOH溶液反应生成白色Al(OH)3絮状沉淀,该沉淀能溶于盐酸或过量的NaOH溶液
(6)Ag+ 能与稀盐酸或可溶性盐酸盐反应,生成白色AgCl沉淀,不溶于稀 HNO3,但溶于氨水,生成〔
Ag(NH3)2〕+。
(7)NH4+ 铵盐(或浓溶液)与NaOH浓溶液反应,并加热,放出使湿润的红色石蓝试纸变蓝的有刺激性
气味NH3气体。
(8)Fe2+ 能与少量NaOH溶液反应,先生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe
(OH)3沉淀。或向亚铁盐的溶液里加入KSCN溶液,不显红色,加入少量新制的氯水后,立即显红色。
2Fe2++Cl2=2Fe3++2Cl-
(9) Fe3+ 能与 KSCN溶液反应,变成血红色 Fe(SCN)3溶液,能与 NaOH溶液反应,生成红褐色Fe
(OH)3沉淀。
(10)Cu2+ 蓝色水溶液(浓的CuCl2溶液显绿色),能与NaOH溶液反应,生成蓝色的Cu(OH)2沉淀,加
热后可转变为黑色的 CuO沉淀。含Cu2+溶液能与Fe、Zn片等反应,在金属片上有红色的铜生成。
几种重要的阴离子的检验
(1)OH- 能使无色酚酞、紫色石蕊、橙色的甲基橙等指示剂分别变为红色、蓝色、**。
(2)Cl- 能与硝酸银反应,生成白色的AgCl沉淀,沉淀不溶于稀硝酸,能溶于氨水,生成[Ag(NH3)
2]+。
(3)Br- 能与硝酸银反应,生成淡**AgBr沉淀,不溶于稀硝酸。
(4)I- 能与硝酸银反应,生成**AgI沉淀,不溶于稀硝酸;也能与氯水反应,生成I2,使淀粉溶
液变蓝。
(5)SO42- 能与含Ba2+溶液反应,生成白色BaSO4沉淀,不溶于硝酸。
(6)SO32- 浓溶液能与强酸反应,产生无色有刺激性气味的SO2气体,该气体能使品红溶液褪色。能与
BaCl2溶液反应,生成白色BaSO3沉淀,该沉淀溶于盐酸,生成无色有刺激性气味的SO2气体。
(7)S2- 能与Pb(NO3)2溶液反应,生成黑色的PbS沉淀。
(8)CO32- 能与BaCl2溶液反应,生成白色的BaCO3沉淀,该沉淀溶于硝酸(或盐酸),生成无色无味
、能使澄清石灰水变浑浊的CO2气体。
(9)HCO3- 取含HCO3-盐溶液煮沸,放出无色无味CO2气体,气体能使澄清石灰水变浑浊或向HCO3-盐
酸溶液里加入稀MgSO4溶液,无现象,加热煮沸,有白色沉淀 MgCO3生成,同时放出 CO2气体。
(10)PO43- 含磷酸根的中性溶液,能与AgNO3反应,生成**Ag3PO4沉淀,该沉淀溶于硝酸。
(11)NO3- 浓溶液或晶体中加入铜片、浓硫酸加热,放出红棕色气体。
这些方程式够用了吧,颜色的话,自己问老师就行
fe的变色反映试验
FeCl3溶液中滴加KSCN溶液显红色
FeCl3能使石蕊变红
FeCl3滴加氢氧化钠溶液生成红褐色沉淀
FeCl3通入H2S生成淡**沉淀
FeCl3加入过量铁粉溶液由棕**变为浅绿色
FeCl3加入过量铜粉溶液变蓝色
FeCl3加入到淀粉——KI溶液中变蓝
FeCl3加入苯酚变紫色
FeCl3加入硝酸银溶液,声称白色沉淀
FeCl3与NaHCO3溶液混合放出气体,并有红褐色沉淀生成
淡**: 硫 Na2O2 AgBr
** :FeS2 AgI Ag3PO4
颜色
石墨 黑色
金刚石 无色
硅 灰黑色
白磷 白或**
红磷 红棕色
硫 淡**
F2 淡黄绿色
Cl2 黄绿色
Br2 深红棕色
I2 紫黑色
铜 紫红色
金 金色
铯 金色
氧化物
NO2红棕色
N2O4无色
Na2O2淡**
FeO黑色
Fe2O3红棕色
Fe3O4黑色
MnO2黑色
CuO黑色
Cu2O红色
HgO红色
Ag2O棕黑色
酸或碱
碱(固体)白色
碱(晶体)无色
Fe(OH)2白色
Fe(OH)3红褐色
Cu(OH)2蓝色
盐
FeS黑色
FeS2**
CuS黑色
Cu2S黑色
HgS黑色
PbS黑色
FeCl3·6H2O 棕褐色
FeSO4·7H2O绿色
CuCl2棕**
CuSO4白色
Cu2(OH)2CO3绿色
CuSO4·5H2O 蓝色
AgCl白色
AgBr淡**
AgI**
Ag2CO3白色
Ag3PO4**
KMnO4紫黑色
水合离子或络离子
Cu2+蓝色
Fe2+浅绿色
Fe3+棕**
MnO4-紫红色
[CuCl4]2- **
Fe(SCN) 2+ 红色
补充CuSO4溶液为蓝色
CuCl2稀溶液溶液为蓝绿色 浓溶液为绿色
常见的焰色反应
含钠元素Na 黄
含锂元素Li 紫红
含钾元素K 浅紫焰色反应(透过蓝色钴玻璃观察,因为钾里面常混有钠,**掩盖了浅紫色)
含铷元素Rb 紫
含钙元素Ca 砖红色
含锶元素Sr 洋红
含铜元素Cu 绿
含钡元素Ba 黄绿
含钴元素Co 淡蓝
含铁元素Fe 无色